Antarcticit
Zur Navigation springen
Zur Suche springen
Autoren: Hans-Jürgen Schwarz
zurück zu Chloride
| Antarcticit'[1][2][3] | |
| |
| Mineralogische Salzbezeichnung | Antarcticit |
| Chemische Bezeichnung | Calciumchlorid Hexahydrat |
| Trivialname | |
| Chemische Formel | CaCl2•6H2O |
| Hydratformen | CaCl2•2H2O (Sinjarit) CaCl2•4H2O (Calciumchlorid-Tetrahydrat) |
| Kristallsystem | trigonal |
| Deliqueszenzfeuchte 20°C | 33,3% |
| Löslichkeit(g/l) bei 20°C | 6,712 mol/kg |
| Dichte (g/cm³) | 1,71 g/cm³ |
| Molares Volumen | 128,0 cm3/mol |
| Molare Masse | 219,07 g/mol |
| Transparenz | |
| Spaltbarkeit | vollkommen |
| Kristallhabitus | |
| Zwillingsbildung | |
| Phasenübergang | |
| Chemisches Verhalten | |
| Bemerkungen | hygroskopisch bis zerfließend |
| Kristalloptik | |
| Brechungsindices | no =1,417-1,495 ne = 1,393-1,550 |
| Doppelbrechung | Δ= 0,055 |
| Optische Orientierung | einachsig negativ |
| Pleochroismus | |
| Dispersion | |
| Verwendete Literatur | |
| [Steiger.etal:2014]Titel: Weathering and Deterioration Autor / Verfasser: Steiger, Michael; Charola A. Elena; Sterflinger, Katja  [Broul.etal:1981]Titel: Solubility in organic two component systems [Broul.etal:1981]Titel: Solubility in organic two component systemsAutor / Verfasser: Broul M., Nyvlt J.; Soehnel O. 
| |
Hygroskopizität[Bearbeiten]
Zur Demonstration der Hygroskopizität von Salzlösungen wurde ein Becher mit konzentrierter CaCl2-Lösung mit einem Becher mit H2O in einen geschlossenen Raum gebracht und beobachtet. Das Video zeigt was geschehen ist. Dauer ca. 3 Tage.
| 0°C | 10°C | 20°C | 30°C | 40°C | 50°C |
| 44,3%r.F. | 39,4%r.F. | 33,3%r.F. | 21,6%r.F. (CaCl2•4H2O) | 18,4%r.F. (CaCl2•4H2O) | 16,3%r.F. (CaCl2•2H2O) |
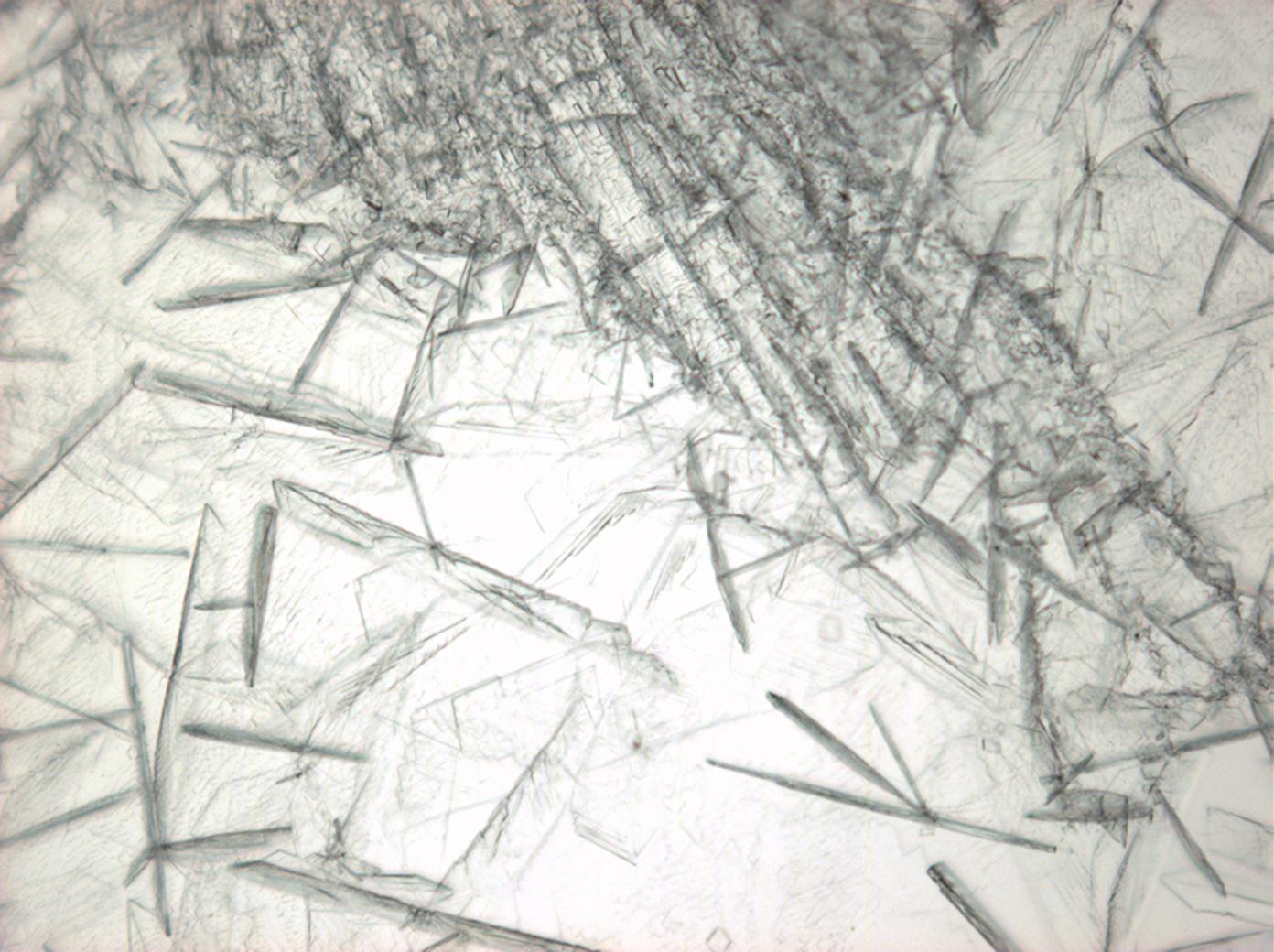
Unter dem Polarisationsmikrokop[Bearbeiten]
- in einfach polarisiertem Licht
- unter gekreuzten Polarisatoren
- unter gekreuzten Polarisatoren (Rot I)
Weblinks[Bearbeiten]
- ↑ http://webmineral.com/data/Antarcticite.shtml gesehen 29.07.2010
- ↑ http://www.mindat.org/min-251.html gesehen 29.07.2010
- ↑ http://www.mineralienatlas.de/lexikon/index.php/MineralData?mineral=Antarcticit gesehen 29.07.2010
Literatur[Bearbeiten]
| [Broul.etal:1981] | Elsevier (Hrsg.) Broul M., Nyvlt J.; Soehnel O. (1981): Solubility in organic two component systems, Elsevier |  |
| [DAns:1933] | d'Ans, J. (1933): Die Lösungsgleichgewichte der Systeme der Salze ozeanischer Salzablagerungen, Verlagsgesellschaft für Ackerbau, M.B.H. Berlin |  |
| [Steiger.etal:2014] | Steiger, Michael; Charola A. Elena; Sterflinger, Katja (2014): Weathering and Deterioration. In: Siegesmund S.; Snethlage R. (Hrsg.): Stone in Architecture, Springer Verlag Berlin Heidelberg, 223-316, Webadresse, https://doi.org/10.1007/978-3-642-45155-3_4. |  |